Tóm tắt
Chi Thiên niên kiện (Homalomena) là nguồn dược liệu quý với nhiều hoạt tính sinh học, trong đó loài H. occulta đã được sử dụng trong y học cổ truyền. Tuy nhiên, các nghiên cứu về thành phần hóa học và hoạt tính ở Việt Nam còn hạn chế, đặc biệt là trên các loài ít phổ biến như H. perplexa, H. pierreana và H. pendula. Các mẫu Thiên niên niên được thu hái và đánh giá chất lượng theo tiêu chuẩn Dược điển Việt Nam V về các chỉ tiêu độ ẩm, độ tro toàn phần và hàm lượng tinh dầu. Cao chiết ethanol 96% từ các mẫu được sử dụng để định lượng hàm lượng polyphenol và flavonoid toàn phần bằng phương pháp đo quang phổ UV-Vis. Hoạt tính kháng oxy hóa được đánh giá thông qua thử nghiệm bắt gốc tự do DPPH so sánh với chất đối chứng Vitamin C.
Kết quả cho thấy cả 4 mẫu đều đạt yêu cầu về độ ẩm và độ tro. Tuy nhiên, hàm lượng tinh dầu biến động, giảm dần theo thứ tự H. perplexa (1,33%), H. pendula (0,82%), H. occulta (0,71%), H. pierreana (0,38%). Hàm lượng polyphenol và flavonoid cao nhất được ghi nhận ở mẫu H. perplexa (lần lượt là 8,03 mg GAE/g và 2,37 mg QE/g), và thấp nhất ở H. occulta. Hoạt tính kháng oxy hóa tương quan thuận với hàm lượng các hợp chất flavonoid và polyphenol, trong đó H. perplexa và H. pendula thể hiện hoạt tính mạnh nhất (IC50 lần lượt là 96,38 và 89,78 µg/mL).
Nghiên cứu đã cung cấp cơ sở dữ liệu khoa học quan trọng, khẳng định sự khác biệt giữa các loài và làm nổi bật tiềm năng của H. perplexa và H. pendula như những nguồn chất chống oxy hóa tự nhiên đầy hứa hẹn, mở ra hướng nghiên cứu chuyên sâu để khai thác và phát triển các ứng dụng dược liệu trong tương lai.
Từ khóa: Chi Thiên niện kiện, thành phần khóa học, DPPH.
1. ĐẶT VẤN ĐỀ
Trong những thập niên gần đây, các nghiên cứu và phát triển thuốc có nguồn gốc từ tự nhiên đã trở thành một trong những hướng tiếp cận trọng tâm của khoa học phát triển dược liệu hiện đại. Việc tìm kiếm, phân lập và đánh giá các hợp chất tự nhiên có hoạt tính sinh học không chỉ góp phần mở rộng dữ liệu về các hoạt chất tiềm năng mà còn đáp ứng xu thế phát triển các sản phẩm an toàn, hiệu quả và thân thiện với môi trường.
Chi Thiên niên kiện (Homalomena) là nhóm thực vật thân thảo lâu năm thuộc họ Ráy (Araceae), bao gồm khoảng 140 loài, phân bố chủ yếu ở Đông Nam Á, Nam Thái Bình Dương và Nam Mỹ (Ye et al., 2017). Theo các tài liệu về cây thuốc Việt Nam, một số loài trong chi Homalomena đã được dùng để điều trị các bệnh về đau nhức xương khớp, đau lưng mỏi gối và hỗ trợ tiêu hóa. Thiên niên kiện (H. occulta) dùng chữa phong thấp, khớp xương đau nhức, co quắp, tê dại, dùng trong trường hợp người già bị đau người, đau dạ dày. Các nghiên cứu dược lý hiện đại còn cho thấy dịch chiết và các hợp chất phân lập từ những loài thuộc chi Homalomena thể hiện nhiều hoạt tính sinh học quan trọng như kháng khuẩn, chống oxy – hóa, gây độc tế bào ung thư và kháng viêm. Nhờ sự đa dạng về loài và đặc tính hóa học phong phú, chi Homalomena được xem là nguồn tài nguyên thực vật có giá trị cao, mở ra triển vọng cho việc sàng lọc và phát triển các hợp chất sinh học mới.
Mặc dù chi Homalomena đã được ghi nhận với nhiều loài có tiềm năng sinh học, nhưng tại Việt Nam, các nghiên cứu về thành phần hóa học và hoạt tính sinh học của chi này vẫn còn hạn chế. Sự thiếu hụt dữ liệu định tính và định lượng về các hợp chất đặc trưng đã cản trở việc khai thác và ứng dụng hiệu quả trong phát triển chế phẩm y dược tự nhiên. Xuất phát từ thực tiễn đó,việc nghiên cứu thành phần hóa học và khảo sát khả năng kháng oxy – hóa của một số loài thuộc chi Thiên niên kiện (Homalomena) tại Việt Nam góp phần để xây dựng nên cơ sở dữ liệu hoàn thiện cho các loài thuộc chi Thiên niên kiện tại Việt Nam tạo tiền đề cho các nghiên chuyên sâu hơn.
2. ĐỐI TƯỢNG VÀ PHƯƠNG PHÁP NGHIÊN CỨU
2.1. Đối tượng nghiên cứu
Nguyên liệu: Tiến hành khảo sát và thu thập mẫu của bốn loài thuộc chi Thiên niên kiện (Homalomena) hiện đang được bảo tồn tại Vườn bảo tồn gene và giống cây thuốc khu vực Nam Bộ, bao gồm: H. pierreana, H. occulta, H. pendula và H. perplexa. Đem các mẫu về Trung tâm Sâm và Dược liệu, TP. Hồ Chí Minh và ghi chú các mẫu lần lượt là: Homalomena occulta (Mẫu TNK-1), Homalomena perplexa (Mẫu TNK-2), Homalomena pierreana (Mẫu TNK-3), Homalomena pendula (Mẫu TNK-4) để tiến hành nghiên cứu.
Chiết cao: Từ mỗi mẫu Thiên niên kiện ban đầu, tiến hành xay nhỏ đến kích thước khoảng 2 mm. Cân chính xác 20 g mẫu, sau đó đem ngâm kiệt với cồn ethanol 96%. Thông số chiết xuất bao gồm tỷ lệ dược liệu: dung môi là 1:20, thời gian ngâm chiết là 24 giờ, tốc độ rút dịch chiết 0,5 mL/phút. Cô dịch chiết bằng máy cô quay ở nhiệt độ 70o đến khi thu được dịch đậm đặc. Tiếp tục cô dịch trên bếp cách thủy đến khi độ ẩm dưới 20% thì thu cao. Cao đặc thu được được sử dụng cho các thử nghiệm tiếp theo.
Hóa chất – thuốc thử : Cồn ethanol 96%, methanol, thuốc thử ether, thuốc thử vanilin, dung dịch acid sulfuric, cyclohexan, ethyl acetat, dung dịch Na2CO3, thuốc thử AlCl3 (Xilong), thuốc thử Folin (Merck), chuẩn acid gallic (Sigma-Aldrich), chuẩn quercetin (Sigma-Aldrich), DPPH(TCI), nước cất.
Chất đối chứng: Acid ascorbic – vitamin C (Sigma-Aldrich), methanol.
2.2. Phương pháp nghiên cứu
2.2.1. Kiểm nghiệm thành phần hóa học các mẫu Thiên niên kiện
Định tính: Cho 10 mL thuốc thử ether vào 1 g dược liệu, lắc 30 phút rồi lọc. Lấy 1 mL dịch lọc, bốc hơi dung môi ở nhiệt độ phòng đến cắn. Thêm vào cắn 1 – 2 giọt dung dịch thuốc thử vanilin 1% trong acid sulfuric. Quan sát sự xuất hiện màu đỏ tía.
Độ ẩm:
Dụng cụ bao gồm: Bình cầu 500 mL, bộ phận xác định lượng nước (bầu ngưng tụ, ống dẫn hơi, và ống hứng chia vạch), ống sinh hàn và nguồn nhiệt (sử dụng bếp điện).
Rửa sạch ống hứng và ống sinh hàn với nước rồi làm khô. Thêm 200 mL toluen và khoảng 2 mL nước vào bình cầu khô. Cất khoảng 2 giờ, để nguội trong 30 phút rồi đọc thể tích nước cất được ở ống hứng (V1), chính xác đến 0,05 mL. Thêm vào bình cầu một lượng mẫu thử đã cân chính xác tới 0,01 g có chứa khoảng 2 – 3 mL nước. Thêm vài mảnh đá bọt. Ðun nóng nhẹ trong 15 phút, khi toluen đã bắt đầu sôi thì điều chỉnh nhiệt để cất với tốc độ 2 giọt dịch cất trong 1 giây. Khi đã cất được phần lớn nước sang ống hứng thì nâng tốc độ cất lên 4 giọt dịch cất trong 1 giây. Tiếp tục cất cho đến khi mực nước cất được trong ống hứng không tăng lên nữa. Dùng 5 – 10 mL toluen rửa thành trong ống sinh hàn. Cất thêm 5 phút nữa. Tách bộ phận cất ra khỏi nguồn cấp nhiệt, để cho ống hứng nguội đến nhiệt độ phòng. Nếu còn có những giọt nước đọng lại trên thành ống sinh hàn thì dùng 5 mL toluen để rửa kéo xuống. Khi lớp nước và lớp toluen đã được phân tách hoàn toàn, đọc thể tích nước trong ống hứng (V2). Thao tác các mẫu phải tiến hành lặp lại 3 lần.
Ðộ ẩm (X %) của dược liệu được tính theo công thức sau:
Trong đó:
V1: Số mL nước cất được sau lần cất đầu.
V2: Số mL nước cất được sau lần cất thứ hai.
p: Số g mẫu đã cân đem thử.
Độ tro toàn phần:
Nung một chén nung bằng sứ cho tới khối lượng không đổi, để nguội trong bình hút ẩm và cân khối lượng của chén. Cân chính xác khoảng 2 g dược liệu cho vào chén nung. Trải đều dược liệu ở đáy chén và đốt cẩn thận trên bếp điện cho đến khi dược liệu cháy hoàn toàn và chén không còn bốc khói. Đặt chén vào lò nung ở 550o cho đến khi vô cơ hóa hoàn toàn (tro không còn màu đen). Dùng cặp sắt lấy chén nung ra, để nguội khoảng 30 phút trong bình hút ẩm. Cân và ghi lại lượng cân. Đặt chén đựng tro vào lò nung và lại tiếp tục nung ở nhiệt độ trên trong 1 giờ nữa. Lấy chén ra, để nguội khoảng 30 phút trong bình hút ẩm. Cân và ghi nhận kết quả. Tiếp tục làm như vậy cho đến khi kết quả 2 lần cân liên tiếp giống nhau hoặc chênh lệch nhau nhiều nhất 0,5 mg.
Tro toàn phần tính trên dược liệu khô kiệt theo công thức:
Trong đó:
A: Tro toàn phần của dược liệu (%)
a: Khối lượng bột trước khi nung (đã trừ ẩm) (g)
b: Khối lượng bột sau khi nung (g).
Hàm lượng tinh dầu:
Sử dụng bộ dụng cụ định lượng tinh dầu nhẹ hơn nước 1000 mL, Đức. Bao gồm: bình cất (bình cầu 1000 mL), bộ dụng cụ cất (ống hứng tinh dầu nhẹ hơn nước, ống sinh hàn và nguồn nhiệt (sử dụng bếp điện).
Tiến hành cân 50 g mẫu bột dược liệu (cân chính xác tới 0,01 g) cho vào bình cất. Thêm 300 mL nước và vài mảnh đá bọt. Lắp bình cất với bộ dụng cụ cất. Ðun bình cho đến sôi, sau đó điều chỉnh tốc độ cất sao cho cất được 1 – 3 mL dịch cất trong 1 phút. Cất liên tục trong 4 giờ. Ngừng cất, sau ít nhất 10 phút đọc thể tích tinh dầu cất được ở ống hứng chia độ. Để tạo sự đồng nhất, cân chính xác các điều kiện (cùng cân, nhiệt độ, áp suất...) và cất đúng 4 giờ với 300 mL nước cất. Tiến hành lặp lại 3 lần cho mỗi mẫu dược liệu.
Công thức tính hàm lượng tinh dầu (tính theo dược liệu khô kiệt):
Trong đó:
X: Hàm lượng phần trăm tinh dầu (%)
a: Thể tích tinh dầu đọc được sau khi cất (mL)
b: Khối lượng dược liệu đã trừ độ ẩm (g).
Định tính tinh dầu bằng phương pháp sắc ký lớp mỏng: Chuẩn bị tinh dầu của các mẫu lần lượt được hòa trong etyl acetat làm dịch chấm. Bản mỏng chấm sắc ký là bản mỏng tráng sẵn silicagel 60 F254 của Đức. Hệ dung môi cyclohexan - ethyl acetat theo tỷ lệ là 8:2. Phun thuốc thử vanilin 2% trong acid sulfuric, sấy bản mỏng ở 105o trong vài phút đến khi hiện rõ các vết trên bản mỏng. Quan sát dưới ánh sáng thường.
2.2.2. Khảo sát hàm lượng polyphenol và flavonoid trong các mẫu cao
Xác định hàm lượng polyphenol trong các mẫu cao:
Xây dựng đường tuyến tính acid gallic: Chuẩn bị dung dịch chuẩn gốc acid gallic 1000 mg/mL. Từ dung dịch chuẩn gốc pha thành các mẫu thử có nồng độ acid gallic từ 10 – 80 mg/mL. Thực hiện phản ứng tạo màu với thuốc thử Folin - Ciocalteu theo quy trình tiêu chuẩn. Sau thời gian phản ứng, đo độ hấp thụ của các mẫu tại bước sóng 765 nm bằng máy quang phổ UV-Vis. Giá trị đo được sử dụng để xây dựng đường chuẩn và tính toán hàm lượng polyphenol toàn phần trong mẫu cao đã thu, biểu thị theo tương đương acid gallic (mg GAE/g mẫu).
Định lượng hàm lượng polyphenol toàn phần trong các mẫu cao: Lần lượt chuẩn bị các dung dịch gốc nồng độ 10 mg/mL tương ứng với cao toàn phần và các cao phân đoạn. Từ các dung dịch gốc trên pha thành các dung dịch có nồng độ phù hợp làm mẫu thử. Hỗn hợp phản ứng bao gồm 1,0 mL dịch thử, 5,0 mL thuốc thử Folin - Ciocalteu đã pha loãng trong vòng 3 phút đến 8 phút. Sau đó thêm 4,0 mL dung dịch Na2CO3 7,5%, để yên ở nhiệt độ phòng trong 60 phút. Tiến hành đo độ hấp thụ quang của dung dịch ở bước sóng 765 nm. Mẫu trắng được chuẩn bị bằng cách thay dung dịch mẫu thử bằng nước cất. Hàm lượng polyphenol toàn phần được biểu diễn bằng đương lượng acid gallic dựa trên đường tuyến tính thể hiện sự phụ thuộc độ hấp thu theo nồng độ acid gallic hay còn được biểu diễn dưới dạng mg GAE/g có nghĩa là mg acid gallic tương đương trên gam cao đặc (Tiêu chuẩn ISO 14502 – 1, 2005).
Xác định hàm lượng flavonoid trong các mẫu cao:
Xây dựng đường tuyến tính quercetin: Chuẩn bị dung dịch chuẩn gốc quercetin có nồng độ 1 mg/mL. Từ dung dịch chuẩn gốc pha thành các dãy mẫu thử có nồng độ quercetin 10 mg/mL, 20 mg/mL, 30 mg/mL, 40 mg/mL, 50 mg/mL và 60 mg/mL. Hút chính xác 1,0 mL mỗi mẫu, thêm vào 1,0 mL dung dịch AlCl3 2% và 8,0 mL methanol, đem ủ 10 phút. Sau khi phản ứng trong điều kiện ủ tối, đo độ hấp thụ tại bước sóng 450 nm bằng máy quang phổ UV-Vis.
Định lượng flavonoid toàn phần trong các mẫu cao: Chuẩn bị các dung dịch gốc cao toàn phần và các cao phân đoạn có nồng độ 10 mg/mL. Từ các dung dịch gốc trên pha này các dung dịch có nồng độ phù hợp làm mẫu thử. Hút chính xác 1 mL mỗi dung dịch mẫu thử, thêm vào 1,0 mL dung dịch AlCl3 2% và 8,0 mL methanol, ủ trong 10 phút. Tiến hành đo quang ở bước sóng 450 nm. Mẫu trắng được chuẩn bị bằng cách thay dung dịch mẫu thử bằng nước cất. Hàm lượng flavonoid toàn phần được ước lượng theo đương lượng quercetin dựa trên đường tuyến tính thể hiện sự phụ thuộc độ hấp thu theo nồng độ quercetin (He at el., 2018).
2.2.4. Khảo sát hoạt tính kháng oxi – hóa trên các mẫu cao bằng thử nghiệm DPPH
Chuẩn bị dung dịch thử: Cân chính xác 10 mg các mẫu cao hòa tan trong methanol và định mức đến 10 mL được dung dịch thử có nồng độ 1000 µg/mL. Từ dung dịch này, tiến hành pha loãng với methanol để thu thành dãy các dung dịch có nồng độ thích hợp phục vụ cho thử nghiệm hoạt tính kháng oxi - hóa.
Thử nghiệm DPPH: Thành phần hỗn hợp có 0,5 mL dung dịch thử trộn với 0,5 mL DPPH 0,6 mM, sau đó thêm 4,0 mL methanol. Hỗn hợp phản ứng được ủ ở nhiệt độ thường, tránh ánh sáng tuyệt đối trong 30 phút. Đo độ hấp thu của mẫu thử ở bước sóng 517 nm. Mẫu đối chứng âm được chuẩn bị bằng cách thay dung dịch mẫu thử bằng methanol. Mẫu đối chứng dương được chuẩn bị bằng cách thay thế dung dịch mẫu thử bằng các dung dịch acid ascorbic (vitamin C) có dãy nồng độ thích hợp. (Mayur et al., 2010).
Xác định giá trị IC50 dựa trên phương trình tuyến tính của từng loại cao. Acid ascorbic (vitamin C) được dùng làm chất đối chứng dương. Thử nghiệm được lặp lại 3 lần với mỗi mẫu thử và lấy giá trị trung bình để tính toán.
Tính toán: Phần trăm bắt gốc tự do tính theo công thức: [(Achứng - Athử)/Achứng] x 100.
3. KẾT QUẢ NGHIÊN CỨU
3.1. Kết quả đánh giá chất lượng dược liệu của một số loài thuộc chi Thiên niên kiện (Homalomena) ở Việt Nam (theo Dược điển Việt Nam V - chuyên luận Thiên niên kiện)

Hình 3.1. Hình ảnh các mẫu Thiên niên kiện.
Định tính: Các mẫu Thiên niên kiện đều có phản ứng dương tính với thuốc thử vanilin 1% trong acid sulphuric. Đạt theo yêu cầu DĐVN V, ghi nhận ở Bảng 3.1
Bảng 3.1. Kết quả định tính các mẫu Thiên niên kiện
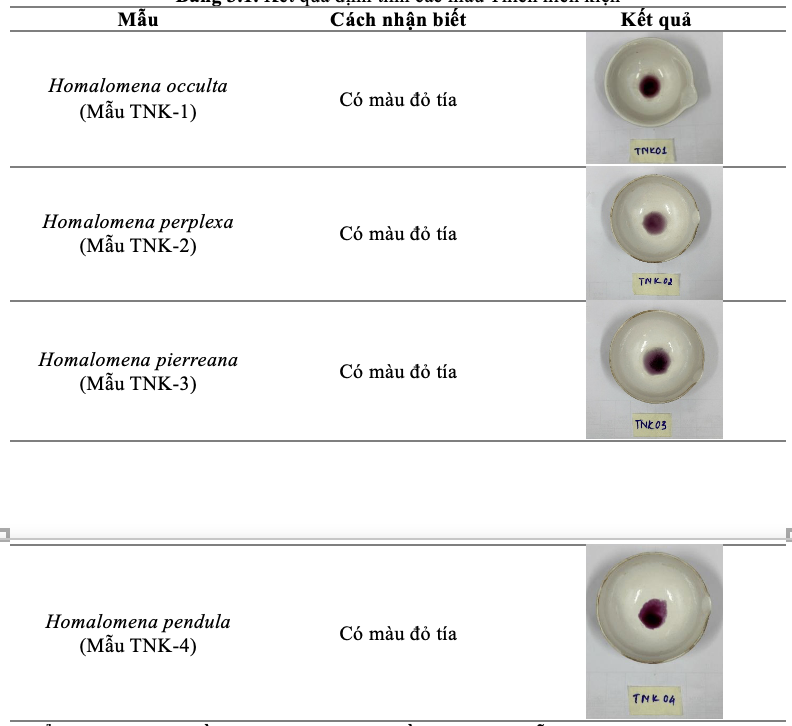
Độ ẩm, độ tro toàn phần và hàm lượng tinh dầu trong các mẫu Thiên niên kiện:
Bảng 3.2. Kết quả đo các thành phần trong các mẫu Thiên niên kiện
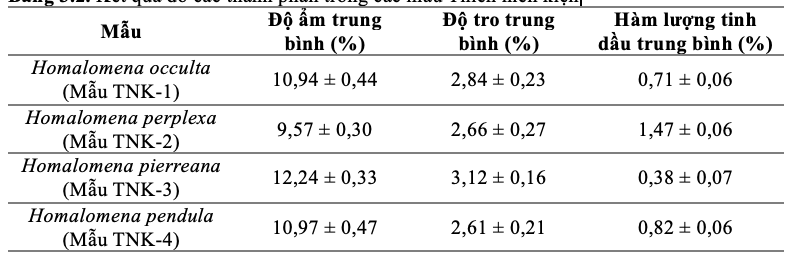
Nhận xét
Độ ẩm các mẫu:
- Độ ẩm trung bình của mẫu Homalomena occulta (TNK-1) là 10,94 % < 14%, mẫu H. occulta đạt độ ẩm theo yêu cầu Dược điển Việt Nam V. Độ ẩm trung bình của mẫu Homalomena perplexa (TNK-2) là 9,57% < 14%, mẫu H. perplexa đạt độ ẩm theo yêu cầu Dược điển Việt Nam V. Độ ẩm trung bình của mẫu Homalomena pierreana (TNK-3) là 12,24% < 14%, mẫu H. pierreana đạt độ ẩm theo yêu cầu Dược điển Việt Nam V. Độ ẩm trung bình của mẫu Homalomena pendula (TNK-4) là 10,97% < 14%, mẫu H. pendula đạt độ ẩm theo yêu cầu Dược điển Việt Nam V (Bảng 3.2).
Độ tro toàn phần:
- Độ tro trung bình của mẫu Homalomena occulta (TNK-1) là 2,84% < 4,0%, mẫu H. occulta đạt độ tro theo yêu cầu Dược điển Việt Nam V. Độ tro trung bình của mẫu Homalomena perplexa (TNK-2) là 2,66 % < 4,0%, mẫu H. perplexa đạt độ tro theo yêu cầu Dược điển Việt Nam. Độ tro trung bình của mẫu Homalomena pierreana (TNK-3) là 3,12% < 4,0%, mẫu H. pierreana đạt độ tro theo yêu cầu Dược điển Việt Nam V. Độ tro trung bình của mẫu Homalomena pendula (TNK-4) là 2,61% < 4,0%, mẫu H. pendula đạt độ tro theo yêu cầu Dược điển Việt Nam V (Bảng 3.2).
Hàm lượng tinh dầu:
- Hàm lượng tinh dầu trung bình của mẫu Homalomena occulta (TNK-1) là 0,71% > 0,5%, mẫu H. occulta đạt yêu cầu định lượng theo yêu cầu Dược điển Việt Nam V. Hàm lượng tinh dầu trung bình của mẫu Homalomena perplexa (TNK-2) là 1,33% > 0,5%, mẫu H. perplexa đạt yêu cầu định lượng theo yêu cầu Dược điển Việt Nam V. Hàm lượng tinh dầu trung bình của mẫu Homalomena pierreana (TNK-3) là 0,38% < 0,5%, mẫu H. pierreana không đạt yêu cầu định lượng theo yêu cầu Dược điển Việt Nam V. Hàm lượng tinh dầu trung bình của mẫu Homalomena pendula (TNK-4) là 0,82% > 0,5%, mẫu H. pendula đạt yêu cầu định lượng theo yêu cầu Dược điển Việt Nam V, kết quả được thể hiện qua Bảng 3.2.
Định tính tinh dầu bằng phương pháp sắc ký lớp mỏng:
Nhìn chung, trên sắc ký đồ mẫu thử là tinh dầu các mẫu Thiên niên kiện phản ứng với thuốc thử vanilin 2% trong acid sulfuric có xuất hiện các vết có màu từ xanh đến hồng, tím có các giá trị Rf từ 0,13 đến 0,85 đặc trưng cho các cấu tử hiện diện trong tinh dầu Thiên niên kiện. Các vết màu và giá trị Rf thu được phù hợp với đặc trưng của các cấu tử có trong tinh dầu Thiên niên kiện, cho thấy cả bốn mẫu thử đều đạt yêu cầu. Kết quả được thể hiện từ Hình 3.2 đến Hình 3.5.

Hình 3.2. Sắc ký đồ mẫu tinh dầu TNK-1 Hình 3.3. Sắc ký đồ mẫu tinh dầu TNK-2
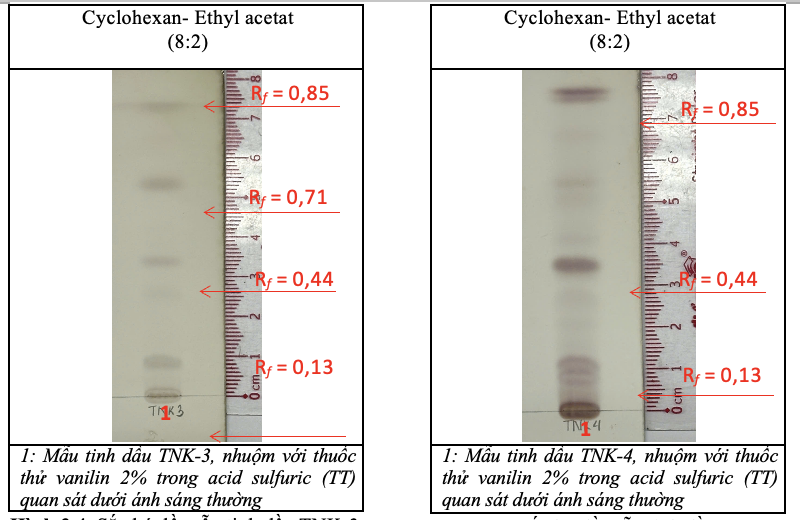
Hình 3.4. Sắc ký đồ mẫu tinh dầu TNK-3 Hình 3.5. Sắc ký đồ mẫu tinh dầu TNK-4
3.2. Kết quả khảo sát hàm lượng polyphenol và flavonoid trong cao chiết một số loài thuộc chi Thiên niên kiện (Homalomena) ở Việt Nam
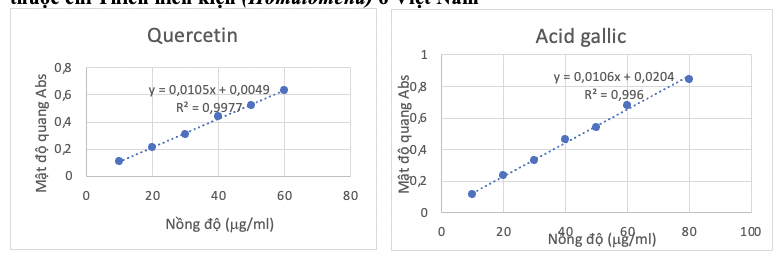
Hình 3.6. Đường chuẩn quercetin Hình 3.7. Đường chuẩn acid gallic
Bảng 3.3. Kết quả khảo sát hàm lượng polyphenol và flavonoid trong các mẫu cao chiết

Nhận xét: Hàm lượng polyphenol và flavonoid trong các mẫu cao chiết có sự biến thiên và có sự tương quan với nhau. Hàm lượng polyphenol và flavonoid cao nhất ở mẫu TNK-2 (tương ứng với hai hàm lượng lần lượt là 2,37% và 8,03%). Hàm lượng polyphenol và flavonoid thấp nhất ở mẫu TNK-1 (tương ứng với hai hàm lượng lần lượt là 0,97% và 3,21%).
3.3. Kết quả khảo sát hoạt tính kháng oxy hóa một số loài thuộc chi Thiên niên kiện (Homalomena) ở Việt Nam
Bảng 3.4. Kết quả khảo sát hoạt tính kháng oxy hóa trong các mẫu cao chiết

Nhận xét: Các mẫu cao chiết từ các loài thiên niên kiện đều thể hiện hoạt tính kháng oxy hóa trên mô hình DPPH, trong đó mẫu cao chiết TNK-2 và TNK-4 thể hiện hoạt tính kháng oxy hóa gần tương đương nhau và mạnh hơn hai mẫu còn lại. Mẫu cao chiết TNK-1 có hoạt tính kháng oxy hóa yếu nhất. Các mẫu thiên niên kiện thể hiện hoạt tính kháng oxy hóa không bằng so với chứng dương vitamin C.
4. Bàn luận
Kết quả nghiên cứu đã cung cấp những dữ liệu khoa học về chất lượng dược liệu, thành phần hóa học và hoạt tính kháng oxy-hóa của bốn loài thuộc chi Thiên niên kiện (Homalomena) tại thu hái Việt Nam, bao gồm: H. occulta, H. perplexa, H. pierreana và H. pendula.
Về chất lượng dược liệu, kết quả đánh giá theo tiêu chuẩn DĐVN V cho thấy cả 4 mẫu đều đạt yêu cầu về chỉ tiêu độ ẩm ( < 14%) và độ tro toàn phần ( < 4%). Tuy nhiên, hàm lượng tinh dầu lại cho thấy sự biến thiên rõ rệt: trong khi H. occulta (0,71%), H. perplexa (1,33%) và H. pendula (0,82%) có hàm lượng đạt > 0,5% theo DĐVN V, thì riêng H. pierreana (0,38%) thấp hơn so với yêu cầu. Sự khác biệt này có thể bắt nguồn từ các yếu tố nội sinh như đặc điểm di truyền, giai đoạn thu hái, bộ phận sử dụng hoặc các yếu tố ngoại sinh như điều kiện sinh thái và phương pháp bảo quản. Kết quả định tính bằng sắc ký lớp mỏng (TLC) cho thấy sự hiện diện của các cấu tử đặc trưng trong tinh dầu (với các giá trị Rf từ 0,13 đến 0,85 và phản ứng màu đặc trưng với thuốc thử vanilin/H₂SO₄) ở cả 4 mẫu, phù hợp với các báo cáo trước đây về thành phần hóa học phức tạp của tinh dầu Thiên niên kiện, thường chứa các sesquiterpenoid và monoterpenoid (Chen et al., 2018; Boyce & Nguyen, 2015).
Đáng chú ý, hàm lượng các nhóm chất polyphenol và flavonoid toàn phần trong cao chiết ethanol 96% của các loài nghiên cứu cho thấy sự chênh lệch lớn. Mẫu H. perplexa (TNK-2) thể hiện hàm lượng cao vượt trội cả về polyphenol (8,03 mg GAE/g) lẫn flavonoid (2,37 mg QE/g), trong khi mẫu H. occulta (TNK-1) lại có hàm lượng thấp nhất (lần lượt là 3,21 mg GAE/g và 0,97 mg QE/g). Sự biến thiên này hoàn toàn phù hợp với xu hướng chung được ghi nhận trong các nghiên cứu trên thế giới về chi Homalomena. Một nghiên cứu trên loài Homalomena sagittifolia ở Malaysia cũng ghi nhận hàm lượng polyphenol và flavonoid đáng kể và tương quan thuận với hoạt tính kháng oxy hóa mạnh (Zulkipli et al., 2020). Tương tự, nghiên cứu của Raj et al. (2019) trên các loài Homalomena ở Ấn Độ cũng xác nhận sự đa dạng về hàm lượng các hợp chất phenolic giữa các loài khác nhau, củng cố cho luận điểm rằng đặc tính hóa học và hoạt tính sinh học của chi này có sự phụ thuộc rất lớn vào loài.
Hoạt tính kháng oxy hóa được đánh giá thông qua thử nghiệm bắt gốc tự do DPPH cho thấy kết quả phù hợp với hàm lượng polyphenol và flavonoid đã định lượng. Các mẫu cao chiết đều thể hiện khả năng kháng oxy hóa, với giá trị IC50 dao động từ 89,78 đến 380,58 µg/mL. Trong đó, mẫu H. perplexa (TNK-2, IC50= 96,38 µg/mL) và H. pendula (TNK-4, IC50= 89,78 µg/mL) có hoạt tính mạnh nhất và tương đương nhau, trong khi mẫu H. occulta (TNK-1, IC50= 380,58 µg/mL) có hoạt tính yếu nhất. Mặc dù hoạt tính của tất cả các mẫu đều thấp hơn đáng kể so với chất đối chứng dương Vitamin C (IC50 = 4,73 µg/mL) kết quả này vẫn rất có ý nghĩa trong bối cảnh tìm kiếm nguồn chất kháng oxy hóa tự nhiên. Đặc biệt, hoạt tính của TNK-2 và TNK-4 rất có tiềm năng khi so sánh với nhiều loại dược liệu khác. Sự khác biệt về hoạt tính giữa các loài có thể được lý giải bởi sự hiện diện của các dẫn xuất flavonoid và acid phenolic cụ thể với cấu trúc và cơ chế hoạt động khác nhau.
So sánh với các nghiên cứu trong nước, kết quả về hoạt tính kháng oxy hóa của H. occulta là tương đồng với báo cáo của Viện Dược liệu (2007), đã mở rộng phạm vi khảo sát ra 3 loài ít được biết đến hơn là H. perplexa, H. pierreana và H. pendula, qua đó cung cấp những dữ liệu đầu tiên và rất giá trị về các loài này. Việc phát hiện H. perplexa và H. pendula có hoạt tính kháng oxy hóa mạnh và hàm lượng hợp chất phenolic cao hơn cả H. occulta - loài được sử dụng phổ biến trong y học cổ truyền, cho thấy tiềm năng to lớn và chưa được khai thác của các nguồn gene thực vật bản địa.
Kết luận
Nghiên cứu đã thành công trong việc cung cấp một cái nhìn toàn diện và có hệ thống về 4 loài Thiên niên kiện ở Việt Nam, không chỉ khẳng định giá trị từ góc độ kiểm nghiệm chất lượng mà còn làm nổi bật tiềm năng kháng oxy hóa của chúng, đặc biệt là ở hai loài H. perplexa và H. pendula. Sự tương quan rõ rệt giữa hàm lượng polyphenol/flavonoid với hoạt tính kháng oxy hóa củng cố cơ sở khoa học cho việc sử dụng các hợp chất này như những chất chỉ thị sinh học cho hoạt tính. Những phát hiện này tạo tiền đề quan trọng cho các nghiên cứu tiếp theo, bao gồm phân lập và nhận danh cấu trúc các hợp chất phenolic chủ đạo, đánh giá các hoạt tính sinh học khác như kháng khuẩn, kháng viêm, gây độc tế bào ung thư trên các mô hình in vitro và in vivo, cũng như nghiên cứu khả năng ứng dụng trong phát triển các sản phẩm dược phẩm từ nguồn dược liệu quý giá của Việt Nam.
LỜI CẢM ƠN
Nghiên cứu này được thực hiện từ sự tài trợ kinh phí của đề tài cơ sở “Xây dựng cơ sở dữ liệu về thành phần loài thuộc chi Thiên niên kiện (Homalonena), họ Araceae ở Việt Nam”. Các tác giả xin chân thành cảm ơn ban lãnh đạo Viện Dược liệu (Cơ quan chủ quản), Trung tâm Sâm và Dược liệu TP.HCM đã tạo điều kiện và hỗ trợ trong suốt quá trình thực hiện nghiên cứu đã tạo điều kiện và hỗ trợ trong suốt quá trình thực hiện nhiệm vụ.
Tài liệu tham khảo:
1. Ye, J., Yin, P., & Xiao, M. T. (2017). New aromatic compounds from the rhizomes of Homalomena occulta. Phytochemistry Letters, 21, 57-60.
2. Viện Dược liệu. (2016). Danh lục cây thuốc Việt Nam. Nhà xuất bản Khoa học và kỹ thuật, 498-500.
3. Bộ Y tế. Dược Điển Việt Nam V. (2018). Nhà xuất bản Y học, Hà Nội.
4. ISO, I. (2005). 14502-1. Determination of substances characteristic of green and black tea Part 1: Content of total polyphenols in tea-colorimetric method using Folin- Ciocalteu reagent.
5. He, J., Chen, L., Chu, B., & Zhang, C. (2018). Determination of total polysaccharides and total flavonoids in Chrysanthemum morifolium using near-infrared hyperspectral imaging and multivariate analysis. Molecules, 23(9), 2395.
6. Mayur, B., Sandesh, S., Shruti, S., & Sung-Yum, S. (2010). Antioxidant and α glucosidase inhibitory properties of Carpesium abrotanoides L. Journal of Medicinal Plants Research, 4(15), 1547-1553.
7. Boyce, P. C., & Nguyen, V. D. (2015). The Araceae of Vietnam. Aroideana, 38, 34-75.
8. Chen, J., Wang, Z., Wu, J., & He, C. (2018). Chemical constituents and biological activities of plants from the genus Homalomena. Chemistry & Biodiversity, 15(5), e1800025.
9. Mensor, L. L., Menezes, F. S., Leitão, G. G., Reis, A. S., dos Santos, T. C., Coube, C. S., & Leitão, S. G. (2001). Screening of Brazilian plant extracts for antioxidant activity by the use of DPPH free radical method. Phytotherapy Research, 15(2), 127-130.
10. Prior, R. L., Wu, X., & Schaich, K. (2005). Standardized methods for the determination of antioxidant capacity and phenolics in foods and dietary supplements. Journal of Agricultural and Food Chemistry, 53(10), 4290-4302.
11. Raj, S., Jeeva, S., & Prakash, J. W. (2019). Phytochemical screening and antioxidant activity of Homalomena aromatica Schott. Journal of Applied Pharmaceutical Science, 9(04), 083-089.
12. Viện Dược liệu. (2007). Cây thuốc và động vật làm thuốc ở Việt Nam (Tập 1). Nhà xuất bản Khoa học và Kỹ thuật.
13. Zulkipli, I. N., Rajabalaya, R., David, S. R., & Idris, A. (2020). Homalomena sagittifolia: A review of its traditional uses, phytochemistry and pharmacology. Journal of Ethnopharmacology, 263, 113123.
INVESTIGATION OF THE CHEMICAL COMPOSITION OF SEVERAL HOMALOMENA SPECIES
Đinh Truong Son2, Phan Thi Cam Tu3, Nguyen Huu Thin1, Đinh Ngoc Bao,
Ngo Thi Minh Huyen1
* Email: ngominhhuyen129@gmail.com
1. Research center of Gingseng and Medicinal Materials
2. Faculty of Chemical Engineering, Industrial University of Ho Chi Minh City
3. Faculty of Biological Sciences, Nong Lam University, Ho Chi Minh city
ABSTRACT
The Homalomena genus is a valuable source of medicinal materials with numerous biological activities, among which H. occulta has been used in traditional medicine. However, studies on the chemical composition and bioactivity of this genus in Vietnam remain limited, especially for less common species such as H. perplexa, H. pierreana, and H. pendula. Plant samples were collected and their quality was evaluated according to the Vietnamese Pharmacopoeia V for parameters including moisture, total ash, and essential oil content. Ethanol 96% extracts from the samples were used to quantify total polyphenol and flavonoid content using UV-Vis spectrophotometry. Antioxidant activity was assessed via the DPPH free radical scavenging assay, compared with Vitamin C as a standard.
The results indicated that all four samples met the requirements for moisture and total ash content. However, the essential oil content varied, decreasing in the following order: H. perplexa (1.33%), H. pendula (0.82%), H. occulta (0.71%), and H. pierreana (0.38%). The highest levels of polyphenols and flavonoids were recorded in the H. perplexa extract (8.03 mg GAE/g and 2.37 mg QE/g, respectively), while the lowest were found in H. occulta. Antioxidant activity was directly correlated with the content of flavonoid and polyphenol compounds, with H. perplexa and H. pendula exhibiting the strongest activity (IC50 values of 96.38 and 89.78 µg/mL, respectively).
This study provides a significant scientific database, confirming the differences among the species and highlighting the potential of H. perplexa and H. pendula as promising sources of natural antioxidants. It opens avenues for further in-depth research to exploit and develop pharmaceutical applications from these resources in the future.
Key words: Homalomena, chemical compositions, DPPH.
Đinh Trường Sơn - Khoa Công nghệ Hóa học, Trường Đại học Công nghiệp TP. Hồ Chí Minh
Phan Thị Cẩm Tú - Khoa Sinh học, Trường Đại học Nông Lâm TP. Hồ Chí Minh
Nguyễn Hữu Thìn - Trung tâm Sâm và Dược liệu TP. Hồ Chí Minh
Đinh Ngọc Bảo - Trung tâm Sâm và Dược liệu TP. Hồ Chí Minh
Ngô Thị Minh Huyền - Trung tâm Sâm và Dược liệu TP. Hồ Chí Minh




































