TÓM TẮT:
Chi Amanita thuộc họ Amanitaceae là một trong những nhóm nấm đảm quan trọng nhất do bao gồm nhiều loài ngoại cộng sinh có vai trò sinh thái lớn trong hệ sinh thái rừng, đồng thời chứa nhiều loài nấm độc nguy hiểm đối với sức khỏe con người, vì vậy nghiên cứu đa dạng di truyền của chi này có ý nghĩa đồng thời về phân loại học, sinh thái học và an toàn sinh học (Cui et al., 2018; Vetter et al., 2023). Tại Việt Nam, dữ liệu phân tử về Amanita còn tương đối hạn chế, đặc biệt đối với các quần thể phân bố ở khu vực Tây Nguyên, nơi có điều kiện sinh thái đa dạng và giàu tiềm năng về nấm ngoại cộng sinh (To et al., 2025). Trong nghiên cứu này, chúng tôi phân tích thành phần nucleotide và mối quan hệ phát sinh chủng loài của 08 mẫu Amanita thu tại Tây Nguyên, gồm A.battarrae, A. beckeri, A. bisporigera, A. fulva, A. rubescens, A. pachycolea, A. porphyria và A. solitaria, sử dụng vùng ITS-rDNA. DNA tổng số được tách chiết bằng phương pháp CTAB cải tiến, sau đó vùng ITS được khuếch đại bằng cặp mồi ITS1/ITS4. Kết quả cho thấy cả 08 mẫu đều cho DNA tổng số có chất lượng tốt, sản phẩm PCR rõ băng đơn và trình tự ITS có chiều dài dao động từ 512 bp đến 674 bp, với giá trị trung bình khoảng 600,5 bp. Thành phần nucleotide cho thấy các mẫu nghiên cứu giàu AT hơn GC, với %GC dao động từ 39,0% đến 44,1% và giá trị trung bình đạt 41,7%, trong khi %AT trung bình đạt 58,3%. Hệ số tương đồng di truyền giữa các cặp mẫu dao động từ 47,04% đến 79,15%, tương ứng khoảng cách di truyền từ 0,08 đến 0,43, cho thấy bộ mẫu có mức độ đa dạng di truyền khá cao. Phân tích cây phát sinh chủng loài cho thấy 08 mẫu được chia thành 02 nhóm chính, trong đó Amanita fulva tách riêng thành một nhánh và 07 mẫu còn lại tạo thành nhóm lớn thứ hai. Kết quả nghiên cứu khẳng định vùng ITS-rDNA là chỉ thị phân tử hữu ích trong nhận diện và phân tích sơ bộ đa dạng di truyền của các loài Amanita, đồng thời cung cấp dữ liệu ban đầu quan trọng phục vụ công tác phân loại, bảo tồn nguồn gen và nghiên cứu nấm độc ở Việt Nam (Cui et al., 2018; Xing et al., 2024).
1. Đặt vấn đề
Chi Amanita là một trong những chi nấm lớn và quan trọng nhất của họ Amanitaceae, phân bố rộng từ vùng ôn đới đến nhiệt đới và được biết đến như một nhóm điển hình của nấm ngoại cộng sinh trong các hệ sinh thái rừng (Cui et al., 2018; Cai et al., 2024). Bên cạnh vai trò sinh thái trong chu trình dinh dưỡng và tương tác nấm–cây chủ, Amanita còn có ý nghĩa y học rất lớn vì bao gồm nhiều loài nấm độc và nấm gây tử vong, chẳng hạn như A. phalloides, A. virosa và A. bisporigera (Vetter et al., 2023). Phân loại truyền thống của Amanita chủ yếu dựa vào đặc điểm hình thái quả thể như mũ nấm, phiến, vòng, volva và đặc điểm vi thể của bào tử, nhưng cách tiếp cận này thường gặp nhiều khó khăn do sự biến thiên hình thái mạnh dưới tác động của môi trường và giai đoạn phát triển của quả thể (Cui et al., 2018; Yang, 2015). Trong những năm gần đây, vùng ITS của operon rDNA đã được sử dụng rộng rãi như một mã vạch DNA cho nấm, nhờ mức độ biến thiên cao giữa các loài nhưng vẫn đủ bảo tồn trong nội loài để hỗ trợ định danh và phân tích quan hệ di truyền (White et al., 1990; Schoch et al., 2012). Nhiều công trình trên thế giới đã sử dụng ITS kết hợp với các marker khác như nrLSU, RPB2 và TEF1-α để làm rõ quan hệ phát sinh chủng loài trong Amanitaceae và phát hiện nhiều loài ẩn hoặc các trường hợp áp dụng sai tên loài theo hình thái truyền thống (Cui et al., 2018; Liu et al., 2023). Ở Việt Nam, nghiên cứu về Amanita vẫn còn tương đối hạn chế so với tiềm năng đa dạng sinh học thực tế, đặc biệt là dữ liệu phân tử phục vụ phân tích phát sinh và nhận diện các loài có giá trị sinh thái hoặc độc tính cao (To et al., 2025).
Xuất phát từ cơ sở đó, nghiên cứu này được thực hiện nhằm phân tích thành phần nucleotide, đánh giá mức độ đa dạng di truyền và làm rõ cấu trúc phát sinh chủng loài của 08 mẫu Amanita thu tại Tây Nguyên dựa trên vùng ITS-rDNA.
2. Vật liệu và phương pháp nghiên cứu
2.1. Vật liệu nghiên cứu
Vật liệu nghiên cứu gồm 08 mẫu nấm thuộc chi Amanita thu tại khu vực Tây Nguyên, bao gồm các loài A. battarrae, A. beckeri, A. bisporigera, A. fulva, A. rubescens, A. pachycolea, A. porphyria và A. solitaria. Các mẫu được lựa chọn trên cơ sở hình thái và được dùng để tách chiết DNA tổng số, khuếch đại vùng ITS, giải trình tự và phân tích phát sinh loài.
2.2. Phương pháp tách chiết DNA tổng số
DNA tổng số được tách chiết theo phương pháp CTAB của Doyle và Doyle có cải tiến nhỏ nhằm phù hợp với vật liệu nấm thực địa, trong đó mẫu nấm được nghiền trong nitơ lỏng, ủ với đệm CTAB, tách bằng chloroform, kết tủa bằng isopropanol, rửa ethanol và xử lý RNase trước khi kiểm tra trên gel agarose 1% (Doyle & Doyle, 1987).
2.3. Khuếch đại vùng ITS-rDNA
Vùng ITS-rDNA được khuếch đại bằng cặp mồi ITS1 và ITS4, với trình tự mồi lần lượt là TCCGTAGGTGAACCTGCGG và TCCTCCGCTTATTGATATGC (White et al., 1990). Phản ứng PCR được tiến hành với thể tích 15 µl, bao gồm buffer, Mg2+, dNTPs, Taq DNA polymerase, cặp mồi ITS và DNA khuôn, với chu trình nhiệt gồm biến tính ban đầu ở 94°C trong 5 phút, 35 chu kỳ khuếch đại và giai đoạn kéo dài cuối ở 72°C trong 7 phút.
2.4. Giải trình tự và phân tích dữ liệu
Sản phẩm PCR được tinh sạch bằng bộ kit QIAquick, sau đó giải trình tự tại Macrogen và xử lý bằng phần mềm MEGA 6.1 cùng CLC Main Workbench 8 để căn chỉnh trình tự, tính thành phần nucleotide, hệ số tương đồng, khoảng cách di truyền và xây dựng cây phát sinh chủng loài.
3. Kết quả và thảo luận
3.1. Chất lượng DNA tổng số và sản phẩm PCR
Kết quả điện di DNA tổng số cho thấy cả 08 mẫu Amanita đều cho băng DNA rõ, tương đối gọn và ít tạp nhiễm, cho thấy DNA thu được có độ nguyên vẹn tốt và phù hợp cho khuếch đại PCR.
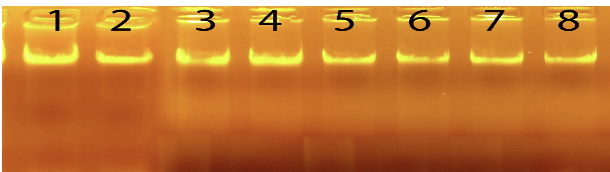
Hình 3.1: Ảnh điện di ADN tổng số của 08 mẫu Nấm (Amanita)
Sản phẩm PCR vùng ITS tạo băng đơn hình rõ trên gel agarose 1,5%, với kích thước xấp xỉ gần 700 bp trước khi tinh sạch, chứng tỏ hệ thống mồi ITS1/ITS4 và điều kiện khuếch đại đã được tối ưu phù hợp cho vật liệu nghiên cứu này.
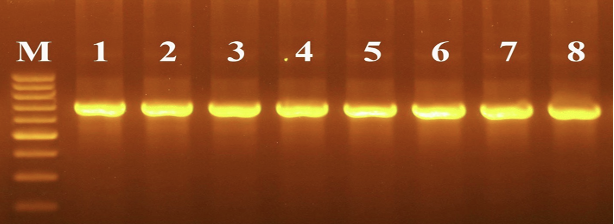
Hình 3.2. Phổ điện di sản phẩm PCR với cặp mồi ITS1/ITS4 trên 8 mẫu Nấm (Amanita) với thang chuẩn Marker: 100bp
Điều đó cho thấy quy trình CTAB cải tiến kết hợp PCR vùng ITS là hướng tiếp cận thích hợp cho phân tích sơ bộ DNA barcode ở các mẫu nấm lớn thu ngoài thực địa tại Việt Nam (Doyle & Doyle, 1987; White et al., 1990).
3.2. Thành phần nucleotide vùng ITS-rDNA
Nghiên cứu thu được 08 trình tự ITS-rDNA với chiều dài dao động từ 512 bp đến 674 bp, giá trị trung bình đạt khoảng 600,5 bp, trong đó A. pachycolea có chiều dài ngắn nhất và A. solitaria có chiều dài dài nhất. Sự khác biệt về chiều dài trình tự cho thấy vùng ITS ở bộ mẫu nghiên cứu có mức độ biến thiên đáng kể, phù hợp với bản chất của vùng spacer trong operon rDNA của nấm, nơi thường xảy ra các biến đổi chèn/xóa và thay thế nucleotide giữa các loài khác nhau (Schoch et al., 2012; Cui et al., 2018).
Phân tích thành phần nucleotide cho thấy tất cả các mẫu đều có tỷ lệ AT cao hơn GC, với %GC dao động từ 39,0% đến 44,1% và giá trị trung bình đạt 41,7%, trong khi %AT dao động từ 55,9% đến 61,0% và đạt trung bình 58,3%. Trong số 08 mẫu, A. battarrae có %GC thấp nhất là 39,0%, còn A. bisporigera có %GC cao nhất là 44,1%. Xu hướng %AT lớn hơn %GC ở vùng ITS-rDNA phù hợp với đặc điểm chung đã được ghi nhận ở nhiều nhóm nấm, bao gồm cả các nghiên cứu DNA barcode và phân tích phát sinh ở Basidiomycota (Schoch et al., 2012).
Bảng 1. Đặc điểm trình tự ITS-rDNA của 08 mẫu nấm Amanita
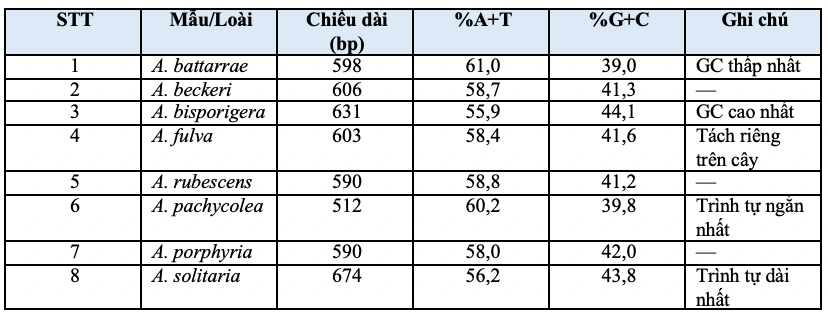
Bảng 1 cho thấy sự khác biệt tương đối rõ về chiều dài trình tự và thành phần base giữa các mẫu, phản ánh mức độ biến thiên nội chi tương đối lớn trong bộ dữ liệu nghiên cứu. Việc trình tự ITS vừa biến thiên về kích thước vừa khác nhau về tỷ lệ GC là cơ sở thuận lợi cho phân tích quan hệ di truyền sơ bộ ở các taxon Amanita.
3.3. Hệ số tương đồng di truyền
Kết quả gióng hàng trình tự cho thấy các sai khác nucleotide giữa 08 mẫu Amanita tập trung chủ yếu ở dạng SNP và xuất hiện rõ trong khoảng 200 nucleotide đầu và 200 nucleotide cuối của chuỗi ITS. Hệ số tương đồng giữa các cặp mẫu dao động từ 47,04% đến 79,15%, cho thấy sự đa dạng di truyền khá lớn trong bộ mẫu nghiên cứu. Khoảng cách di truyền tương ứng dao động từ 0,08 đến 0,43, trong đó giá trị thấp phản ánh các cặp mẫu gần nhau hơn và giá trị cao phản ánh mức phân hóa tương đối lớn giữa các loài trong bộ dữ liệu. Từ góc độ phân loại học, các giá trị tương đồng thấp là tín hiệu mạnh cho thấy vùng ITS đủ nhạy để tách các đại diện Amanita khác biệt trong nghiên cứu này, mặc dù để kết luận ranh giới loài một cách chặt chẽ vẫn cần bổ sung các marker khác như nrLSU, RPB2 hoặc TEF1-α (Cui et al., 2018; Liu et al., 2023).
Bảng 2. Khoảng biến thiên chỉ số di truyền giữa các mẫu Amanita
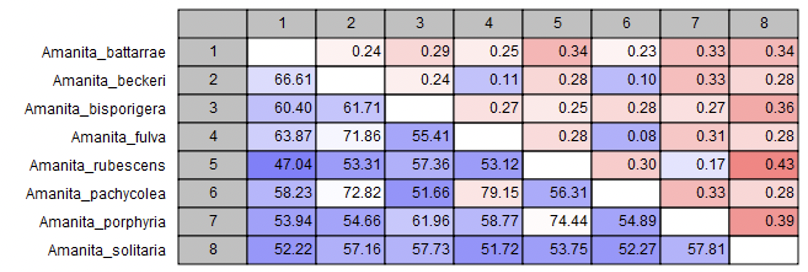
3.4. Cây quan hệ phát sinh chủng loài
Cây phát sinh chủng loài xây dựng từ dữ liệu ITS cho thấy 08 mẫu Amanita được chia thành 02 nhóm chính. Nhóm thứ nhất chỉ gồm Amanita fulva, thể hiện mức độ tách biệt rõ với các mẫu còn lại trong bộ dữ liệu. Nhóm thứ hai bao gồm 07 mẫu còn lại là A. battarrae, A. solitaria, A. porphyria, A. beckeri, A. rubescens, A. pachycolea và A. bisporigera. Cấu trúc này cho thấy ngay cả khi chỉ sử dụng một locus là ITS, dữ liệu vẫn đủ khả năng phân tách các mẫu nghiên cứu thành những cụm phát sinh có ý nghĩa sơ bộ về tiến hóa và quan hệ di truyền nội bộ. Kết quả này phù hợp với các nghiên cứu trước đây cho thấy Amanita là một chi có cấu trúc phát sinh phức tạp, nhiều dòng dõi tiến hóa sâu và mức đa dạng di truyền lớn, đặc biệt khi xét ở quy mô liên loài (Cui et al., 2018; Cai et al., 2024).
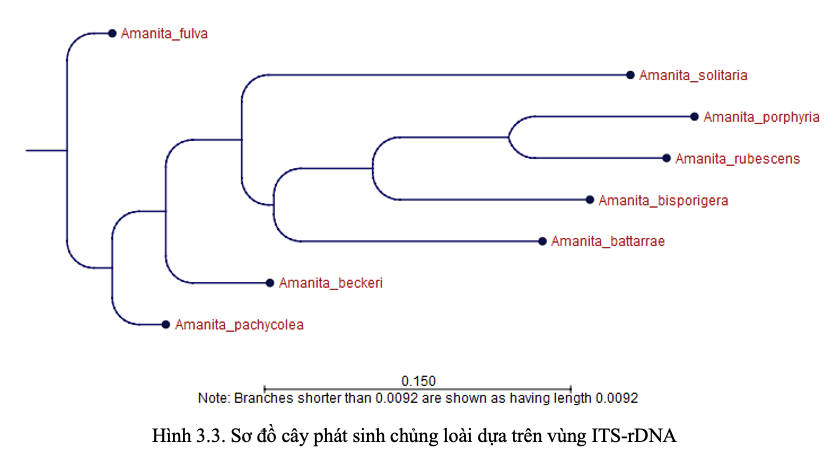
Hình 3.3. Sơ đồ cây phát sinh chủng loài dựa trên vùng ITS-rDNA
3.5. Thảo luận chung
Nghiên cứu cho thấy quy trình tách chiết CTAB cải tiến và hệ thống PCR ITS1/ITS4 có thể áp dụng tốt cho các mẫu Amanita thu ngoài tự nhiên ở Tây Nguyên. Điều này đặc biệt có ý nghĩa trong điều kiện mẫu nấm thực địa thường chứa nhiều polysaccharide và chất chuyển hóa thứ cấp gây khó khăn cho việc tách DNA sạch.
Từ góc nhìn di truyền, thành phần %AT cao hơn %GC và sự biến thiên lớn về chiều dài cũng như trình tự ITS ở bộ mẫu Amanita cho thấy vùng này thích hợp để phân tích đa dạng di truyền sơ bộ trong điều kiện nguồn lực nghiên cứu còn hạn chế. Mức tương đồng thấp giữa một số cặp mẫu cho thấy các đại diện Amanita trong nghiên cứu có mức phân hóa tương đối sâu, đồng thời nhấn mạnh tính đa dạng di truyền đáng kể của chi này tại Việt Nam.
Điều này đặc biệt quan trọng vì Amanita không chỉ là nhóm nấm có giá trị sinh thái mà còn bao gồm các loài nấm độc nguy hiểm, nên bất kỳ dữ liệu phân tử nào giúp nhận diện và phân tách loài đều có ý nghĩa ứng dụng thực tiễn đối với y tế dự phòng và cảnh báo ngộ độc (Vetter et al., 2023; Xing et al., 2024).
Tuy nhiên, nghiên cứu hiện tại vẫn còn một số hạn chế như số lượng mẫu chưa lớn, chưa tích hợp đầy đủ dữ liệu cây chủ và sinh cảnh, đồng thời mới chỉ dựa trên một marker ITS nên chưa đủ để giải quyết triệt để các vấn đề phát sinh sâu trong chi Amanita (Cui et al., 2018; To et al., 2025).
Vì vậy, trong các nghiên cứu tiếp theo cần mở rộng cỡ mẫu trên nhiều vùng sinh thái của Việt Nam, kết hợp ITS với các locus có độ phân giải cao hơn và đối chiếu với dữ liệu tham chiếu quốc tế để xây dựng cơ sở dữ liệu chuẩn cho Amanita Việt Nam (Cui et al., 2018; Cai et al., 2024).
4. Kết luận
Phân tích vùng ITS-rDNA của 08 mẫu Amanita thu tại Tây Nguyên cho thấy DNA tổng số và sản phẩm PCR đều đạt chất lượng tốt, đủ điều kiện cho giải trình tự và phân tích phát sinh chủng loài.
Các trình tự ITS có chiều dài dao động từ 512 bp đến 674 bp và đều có xu hướng giàu AT hơn GC, với %GC trung bình đạt 41,7%.
Hệ số tương đồng di truyền dao động từ 47,04% đến 79,15% và khoảng cách di truyền từ 0,08 đến 0,43 cho thấy mức độ đa dạng di truyền tương đối cao giữa các mẫu nghiên cứu.
Cây phát sinh chủng loài chia 08 mẫu thành 02 nhóm chính, trong đó Amanita fulva tách riêng thành một nhánh và 07 mẫu còn lại tập hợp thành nhóm thứ hai, phản ánh sự khác biệt phát sinh đáng kể trong bộ mẫu khảo sát.
Kết quả nghiên cứu khẳng định tính hữu ích của vùng ITS-rDNA trong nhận diện và phân tích sơ bộ đa dạng di truyền các loài Amanita, đồng thời cung cấp dữ liệu nền cần thiết cho công tác phân loại, bảo tồn và nghiên cứu nấm độc ở Việt Nam (Cui et al., 2018; Xing et al., 2024).
Tài liệu tham khảo
Xing, RR., Bai, WM., Hu, D. et al. Using a DNA mini-barcode within the ITS region to identify toxic Amanita in mushroom poisoning cases. Appl Microbiol Biotechnol 108, 376 (2024). https://doi.org/10.1007/s00253-024-13219-x
Liu, Y. S., Liu, J.-K., Kumla, J., Suwannarach, N., & Lumyong, S. (2023). Taxonomic Novelties and New Records of Amanita Subgenus Amanitina from Thailand. Journal of Fungi, 9(6), 601. https://doi.org/10.3390/jof9060601
Cui, YY., Cai, Q., Tang, LP. et al. The family Amanitaceae: molecular phylogeny, higher-rank taxonomy and the species in China. Fungal Diversity 91, 5–230 (2018). https://doi.org/10.1007/s13225-018-0405-9
Doyle, J.J. and Doyle, J.L. A Rapid DNA Isolation Procedure for Small Quantities of Fresh Leaf Tissue. Phytochemical Bulletin, 19, 11-15 (1987).
Vetter, J. (2023). Amanitins: The Most Poisonous Molecules of the Fungal World. Molecules, 28(15), 5932. https://doi.org/10.3390/molecules28155932
Schoch, C. L., Seifert, K. A., Huhndorf, S., Robert, V., Spouge, J. L., Levesque, C. A., et al. (2012). Nuclear ribosomal internal transcribed spacer (ITS) region as a universal DNA barcode marker for Fungi. Proceedings of the National Academy of Sciences of the United States of America, 109(16), 6241–6246.
To, D. C., Nguyen, P. D., Nguyen, H. K., Dang, T. T. H., Nguyen, V. S., Nguyen, P. H., Tran, T. H., Nguyen, N. P., & Nguyen, H. T. (2025). Ecological factors affecting the distribution of the Amanita genus (poisonous mushrooms) in the Central Highlands, Vietnam. Gayana Botánica, 82(2), 143–155.
Cai Q, Codjia JEI, Buyck B, Cui YY, Ryberg M, Yorou NS, Yang ZL. The evolution of ectomycorrhizal symbiosis and host-plant switches are the main drivers for diversification of Amanitaceae (Agaricales, Basidiomycota). BMC Biol. 2024 Oct 10;22(1):230. doi: 10.1186/s12915-024-02031-8.
White, T. J., Bruns, T. D., Lee, S. B., & Taylor, J. W. (1990). Amplification and direct sequencing of fungal ribosomal RNA genes for phylogenetics. In M. A. Innis, D. H. Gelfand, J. J. Sninsky, & T. J. White (Eds.), PCR protocols: A guide to methods and applications (pp. 315–322). Academic Press.
Yang, Z. L. (2015). Atlas of the Chinese species of Amanitaceae. Science Press.
NUCLEOTIDE COMPOSITION AND PHYLOGENETIC TREE STRUCTURE ANALYSIS OF THE AMANITA COLLECTED FROM THE CENTRAL HIGHLANDS OF VIETNAM
Luu thuy Hoa1, Nguyen Trương Khoa2, Tran Minh Trang3, Nguyen Huu Kien4, Nguyen Phuong Dai Nguyen4
1. Hai Phong University
2. Agricultural Genetics Institute
3. Nguyen Sieu Secondary and High School
4. Tay Nguyen University
ABSTRACT:
The genus Amanita, belonging to the family Amanitaceae, is one of the most important groups of basidiomycete fungi because it includes many ectomycorrhizal species that play major ecological roles in forest ecosystems, while also containing numerous poisonous species that are hazardous to human health. Therefore, research on the genetic diversity of this genus is of significance for taxonomy, ecology, and biosafety (Cui et al., 2018; Vetter et al., 2023). In Vietnam, molecular data on Amanita are still relatively limited, particularly for populations distributed in the Central Highlands, a region with diverse ecological conditions and strong potential for ectomycorrhizal fungi (To et al., 2025). In this study, we analyzed the nucleotide composition and phylogenetic relationships of eight Amanita samples collected from the Central Highlands, including A. battarrae, A. beckeri, A. bisporigera, A. fulva, A. rubescens, A. pachycolea, A. porphyria, and A. solitaria, using the ITS-rDNA region. Total genomic DNA was extracted using a modified CTAB method, and the ITS region was subsequently amplified using the ITS1/ITS4 primer pair. The results showed that all eight samples yielded good-quality total DNA, clear single-band PCR products, and ITS sequences ranging from 512 bp to 674 bp in length, with an average length of approximately 600.5 bp. Nucleotide composition analysis indicated that the studied samples were richer in AT than GC, with GC content ranging from 39.0% to 44.1% and an average of 41.7%, while the average AT content reached 58.3%. Genetic similarity coefficients among sample pairs ranged from 47.04% to 79.15%, corresponding to genetic distances from 0.08 to 0.43, indicating a relatively high level of genetic diversity within the sample set. Phylogenetic tree analysis showed that the eight samples were divided into two major groups, in which Amanita fulva formed a separate branch and the remaining seven samples clustered into the second major group. The results confirm that the ITS-rDNA region is a useful molecular marker for the identification and preliminary analysis of genetic diversity in Amanita species, while also providing important baseline data for taxonomy, germplasm conservation, and poisonous mushroom research in Vietnam (Cui et al., 2018; Xing et al., 2024).
Keywords: Amanita, ITS-rDNA, nucleotide composition, phylogeny, genetic diversity, Central Highlands.
Lưu Thúy Hòa - Đại học Hải Phòng
Nguyễn Trường Khoa - Viện Di truyền Nông nghiệp
Trần Minh Trang - Trường THCS - THPT Nguyễn Siêu
Nguyễn Hữu Kiên - Đại học Tây Nguyên
Nguyễn Phương Đại Nguyên - Đại học Tây Nguyên




































